Odborne vypracovali:
PharmDr. Monika Hammerschmidt,
Mgr. Renáta Kozáčiková.
Chronický deficit horčíka (Mg²⁺), draslíka (K⁺) a koenzýmu Q10 (CoQ10) predstavuje jeden z najviac závažných, avšak súčasne najprehliadanejších problémov súčasnej preventívnej medicíny. Spoločne tieto tri zložky tvoria biochemicky prepojenú funkčnú jednotku: deficit jednej z nich systematicky narúša funkciu zvyšných dvoch. Cieľom tohto článku je preto vysvetliť fyziológiu a vzájomné pôsobenie spomenutých zložiek na základe aktuálnych výskumných dát, analyzovať príčiny a dôsledky ich deficitu, identifikovať rizikové skupiny, ako aj kriticky posúdiť efektivitu ich suplementácie s ohľadom na biologickú dostupnosť jednotlivých foriem.
1. Charakteristika jednotlivých zložiek
Každá z týchto zložiek sa podieľa na odlišnej, avšak komplementárnej vrstve bunkového energetického metabolizmu. Preto je porozumenie vzájomného pôsobenia týchto troch zložiek podmienené pochopením ich individuálnych fyziologických funkcií.
1.1 Horčík (Mg²⁺): esenciálny regulátor bunkovej energie
Horčík predstavuje štvrtý najvýznamnejší katión (kladne nabitý ión) v ľudskom tele. Celková zásoba v organizme u dospelého jedinca dosahuje hodnoty v rozmedzí 20–28 g, pričom z toho okolo 50 %–60 % sa nachádza v kostiach, v svaloch je to približne 34 %–39 % a zvyšných 19 % v ostatných mäkkých tkanivách. Extracelulárna frakcia horčíka cirkulujúca v krvi tvorí menej ako 1 %–2 % celkového množstva, avšak práve táto zložka je biologicky aktívna a meraná laboratórnymi vyšetreniami. Štandardná hodnota sérovej koncentrácie Mg²⁺ sa pohybuje v rozmedzí 0,7–1,1 mmol/l [1].
Na molekulárnej úrovni horčík pôsobí vo vyše 600 enzymatických procesoch ako esenciálny kofaktor a zastáva funkciu aktivátora v ďalších 200 reakciách [2]. Nevyhnutná je jeho interakcia s adenozíntrifosfátom (ATP), univerzálnym intracelulárnym prenášačom energie, ktorý je biologicky aktívny výhradne vo formeMgATP²⁻, teda keď je ATP chemicky viazaný s horčíkom. Absencia tejto väzby spôsobuje, že enzýmy nedokážu ATP účinne rozpoznať a využiť, čo vedie k nevyužitiu energie, ktorá je v ATP uložená a tým nie je dostupná pre mnohé bunkové procesy [3].
Horčík má podstatný vplyv taktiež na nervový systém, kde zasahuje ako fyziologický antagonista (blokátor) NMDA receptorov, ionotropných receptorov pre glutamát, ktoré reagujú na primárny excitačný neurotransmiter CNS (Centrálnej nervovej sústavy). Týmto dokáže horčík brániť nadmernej neuronálnej depolarizácii a excitotoxicite (poškodeniu neurónov nadmernou stimuláciou), ktorá môže viesť až k bunkovej smrti neurónov, poprípade chronickej úzkosti [2].
1.2 Draslík (K⁺): stabilizátor elektrickej vodivosti a funkcie bunkových membrán
Draslík je ďalším dominantným katiónom, ktorého až 98 % (okolo 3500 mmol) celkového množstva sa nachádza vo vnútri buniek. Tým pádom extracelulárna (mimobunková) koncentrácia K⁺ tvorí približne 2 % (65 mmol). Za taktúto koncentračnú nerovnováhu zodpovedá enzým Na⁺/K⁺-ATPáza (sodíko-draslíková pumpa), ktorý hydrolyzuje (štiepi) ATP a tak dokáže v každom cykle zúžitkovať uvoľnenú energiu na transport 3 iónov Na⁺ z bunky a 2 iónov K⁺ do bunky [4]. Výsledný elektrochemický rozdiel katiónov draslíka predstavuje základ pokojového membránového napätia, ktoré je nevyhnutné pre vznik akčného potenciálu (elektrického impulzu šíriaceho sa naprieč nervovými a svalovými tkanivami).
Úbytok intracelulárnej hladiny draslíka spôsobuje depolarizáciu membrány buniek, čo zvyšuje ich elektrickú excitabilitu. V rámci srdcových svalových buniek (kardiomyocytoch) sa to prejavuje zvýšeným rizikom vzniku nebezpečných arytmii (porúch srdcového rytmu) a spontánnych elektrických výbojov [4]. Z tohto dôvodu predstavuje hypokaliémia (pokles hladiny K⁺ pod 3,5 mmol/l) kritickú hrozbu pre vznik komorových arytmií.
Okrem vplyvu na srdce draslík súčasne plní kľúčovú úlohu v regulácii krvného tlaku: podporuje totiž vylučovanie sodíka v obličkách a blokuje aktivitu WNK kinázy (with-no-lysine kináza – regulačný enzým distálneho nefronu obličky), čím efektívne znižuje krvný tlak [5].
1.3 Koenzým Q10 (CoQ10): lipofilný antioxidant a prenášač elektrónov v dýchacom reťazci
Koenzým Q10 je lipofilná molekula (rozpustná v tukoch), ktorú organizmus tvorí v pečeni rovnakým procesom ako cholesterol – prostredníctvom mevalonátovej dráhy (biochemickej kaskády). CoQ10 sa vyskytuje v dvoch chemických formách:
- Ubichinón – oxidovaná forma (CoQ10), ktorá je schopná z dýchacieho reťazca prijímať elektróny
- Ubichinol – redukovaná forma (CoQ10H₂), plní antioxidačnú funkciu a navyše prenáša elektróny ďalej v dýchacom reťazci
V mitochondriálnom dýchacom reťazci CoQ10 zabezpečuje transport elektrónov medzi proteínovými komplexmi I, II a III. Elektróny uvoľnené na komplexoch I a II sa prenášajú na CoQ10, čím sa ubichinón redukuje na ubichinol. Ubichinol potom odovzdáva tieto elektróny komplexu III. Tento proces je nevyhnutný pre syntézu ATP [6]. Bez CoQ10 je táto sekvencia prerušená a tým tvorba ATP dramaticky klesá.
Ubichinol zároveň pôsobí ako zásadný antioxidant, ktorý neutralizuje reaktívne formy kyslíka (ROS — reactive oxygen species; voľné radikály), čím dokáže zabrániť poškodeniu mitochondriálnych membrán, mitochondriálnej DNA a proteínov [6]. Viac sa o tejto forme dočítate v kapitole 6.
2. Biochemické pôsobenie trojice Mg-K-CoQ10
Po pochopení funkcií jednotlivých zložiek je možné analyzovať, prečo je ich vzájomné prepojenie fyziologicky nevyhnutné.
Horčík aktivuje enzýmy Krebsovho cyklu a vo forme MgATP²⁻ poháňa Na⁺/K⁺-ATPázu, ktorá je zodpovedná za udržiavanie intracelulárnej hladiny K⁺. CoQ10 umožňuje prenos elektrónov v dýchacom reťazci, bez ktorého by NADH a FADH₂ produkované Krebsovým cyklom ostali nevyužité a ATP by sa nevyrábalo. Draslík, udržiavaný v bunke funkčnou Na⁺/K⁺-ATPázou, zabezpečuje membránový potenciál srdcových svalových buniek, neurónov a kostrových svalov. Jeho nedostatok spôsobí elektrofyziologickú nestabilitu bez ohľadu na to, či je dostatok ATP alebo CoQ10 [2, 3, 4, 6].
Klinická závislosť horčíka od draslíka a naopak je riadená špecifickými molekulárnymi mechanizmami, kde hypomagneziémia priamo ovplyvňuje deficit draslíka. Nedostatok horčíka limituje funkčnú kapacitu Na⁺/K⁺-ATPázy, čo narúša aktívny transport draslíka do buniek. Súčasne dochádza k strate inhibičného vplyvu vnútrobunkového horčíka na kanál ROMK (renal outer medullary potassium channel – draslíkový kanál vo vonkajšej dreni obličky), čo vedie k zvýšenému vylučovaniu draslíka obličkami a možnému rozvoju sekundárnej hypokaliémie. Z terapeutického hľadiska, suplementácia samotného K⁺ u pacienta s hypomagneziémiou preto nedosahuje žiadaný efekt – hladina draslíka sa môže ustáliť až po úprave deficitu Mg²⁺. Vyše 50 % klinicky závažných hypokaliémií má prítomný súčasný deficit horčíka [4, 5].
Prepojenie medzi koenzýmom Q10 a horčíkom bolo dokumentované pri viacerých ochoreniach, súvisiacich s poruchami mitochondriálnej činnosti, vrátane cukrovky (diabetes mellitus 2. typu), srdcového zlyhania, či vrodenými mitochondriálnymi ochoreniami (mitochondriálna cytopatia). Významným zistením bolo, že pri týchto stavoch boli zaznamenané znížené hladiny Mg²⁺ v tkanivách, avšak zlepšenie mitochondriálnej funkcieprostredníctvom suplementácie CoQ10 normalizovalo aj distribúciu Mg²⁺ v bunke [2]. Tento jav naznačuje, že energetický nedostatok v mitochondriách vyvolaný nedostatkom CoQ10 priamo narúša bunkovú rovnováhu horčíka, čo potvrdzuje, že deficit jednej zložky negatívne ovplyvňuje hladinu tej druhej a naopak.
3. Analýza nedostatku: prejavy deficitu v klinickej praxi
Súbežný nedostatok trojice Mg–K–CoQ10 vyvoláva nešpecifické symptómy, ktoré v lekárskej praxi často unikajú správnej diagnostike alebo sa liečia symptomaticky bez identifikovania nutričnej príčiny. Nasledujúci prehľad popisuje prejavy ich vzájomného deficitu podľa jednotlivých orgánových systémov.
-
- Kardiovaskulárny systém
Súbežný deficit Mg²⁺ a K⁺ zásadne narúša elektrickú stabilitu srdca, čo vedie k zvýšenej náchylnosti na vznik arytmií a čiastočnej depolarizácii membrány kardiomyocytov [4]. Navyše, nedostatok CoQ10znižuje produkciu ATP v myokarde – srdcovom svale, ktorý je jedným z energeticky najnáročnejších orgánov v ľudskom tele. Nedostatok horčíka navyše preukázateľne súvisí s rozvojom vysokého krvného tlaku a celkovým nárastom kardiovaskulárnych rizík [7]. - Nervovosvalový systém
Deficit horčíkaznižuje prah neuromuskulárnej excitability, v dôsledku čoho aj pri minimálnom alebo chýbajúcom nervovom podnete dochádza k sťahom svalových vlákien. Prejavuje sa to najmä nočnými svalovými kŕčmi (predovšetkým v lýtkovej oblasti), svalovou slabosťou, zvýšenou únavou pri fyzickej záťaži a zášklbmi očných viečok (okružného svalu oka) [2]. Súbežný nedostatok draslíka tento stav zhoršuje narušením správnej reakcie svalových buniek na nervové signály, čím prispieva k svalovej slabosti a kŕčom [2]. - Energetický metabolizmus a kognitívne funkcie
Stavy ako chronická únava (napriek adekvátnemu odpočinku), spomalené kognitívne funkcie a emocionálne vyhorenie odrážajú zníženú tvorbu ATP v mitochondriách, predovšetkým v svalových bunkách a neurónoch. Klinické a in vivo štúdie poukazujú na to, že pravidelné užívanie koenzýmu Q10 sa preukázalo ako efektívny spôsob ochrany mozgu pred oxidačným stresom a podpory zvýšenia produkcie ATP v hipokampe a mozgovej kôre (oblastiach zodpovedných za pamäť a učenie). Avšak, v humánnych štúdiách sú výsledky nekonzistentné. Ukazuje sa, že terapeutický prínos je výraznejší u pacientov s už prítomnou mitochondriálnou poruchou (napr. pri srdcovom zlyhávaní alebo cukrovke diabetes mellitus 2. typu), než u zdravých jedincov [8].
Deficit horčíka priamo súvisí s poruchami nálady a duševným zdravím. Štúdia od Tarleton et al. (2017) pri 126 dospelých (priemerný vek 52 rokov) s miernou až stredne ťažkou depresiou preukázala, že užívanie 248 mg horčíka denne počas 6 týždňovviedlo k významnému zlepšeniu stavu pacientov. Pomocou dotazníkov sa nameral pokles skóre depresie (PHQ-9, dotazník pacientov hodnotenia depresie) o 6,0 bodov (CI −7,9 až −4,2; p< 0,001) a skóre úzkosti (GAD-7, dotazník hodnotenia úzkosti) o 4,5 bodov (CI −6,6 až −2,4; p< 0,001) [9]. Efekt sa objavil už do dvoch týždňov a bol nezávislý od veku, pohlavia ani počiatočnej hladiny Mg²⁺. Metaanalýza siedmich randomizovaných klinických štúdií zahŕňajúca 325 dospelých (vo vekovom rozpätí od 20 – 60 rokov) s depresívnou poruchou potvrdila štatisticky významnézmiernenie symptómov depresie pri suplementácii horčíka (štandardizovaný priemerný rozdiel (SMD): −0,919; 95% CI: −1,443 až −0,396; p = 0,001) [10]. Podklad týchto zmien spočíva najmä v schopnosti horčíka regulovať NMDA receptory a glutamátergnej transmisie horčíkom [2].
- Kardiovaskulárny systém
4. Zdroje nutričného deficitu v modernej dobe
Analýza klinických prejavov deficitu prirodzene vedie k jadru problému: prečo v súčasnosti pri vysokej dostupnosti a nadbytku potravín čelíme tak masívnemu nedostatku kľúčových mikroživín? Za tento stav zodpovedá kombinácia mnohých faktorov. Najkritickejšími činiteľmi sú degradácia kvality pôdy a potravín, vplyvy moderného životného štýlu a negatívne pôsobenie niektorých liečív. Nasledujúce podkapitoly tieto jednotlivé faktory systematicky analyzujú.
4.1 Degradácia pôdy a pokles minerálnej hodnoty potravín
Intenzívne poľnohospodárske spracovanie pôdy, ktoré bolo uplatňované od druhej polovice 20. storočia viedlo k podstatnému vyčerpaniu minerálneho bohatstva pôdy. Používaním jednostranných syntetických NPK hnojív (obsahujúcich dusík, fosfor a draslík) ostal prirodzene vyskytujúci sa horčík zanedbaný, k čomu navyše prispieva aj kyslosť pôd a dažde, ktoré tento minerál z pôdy odplavujú.
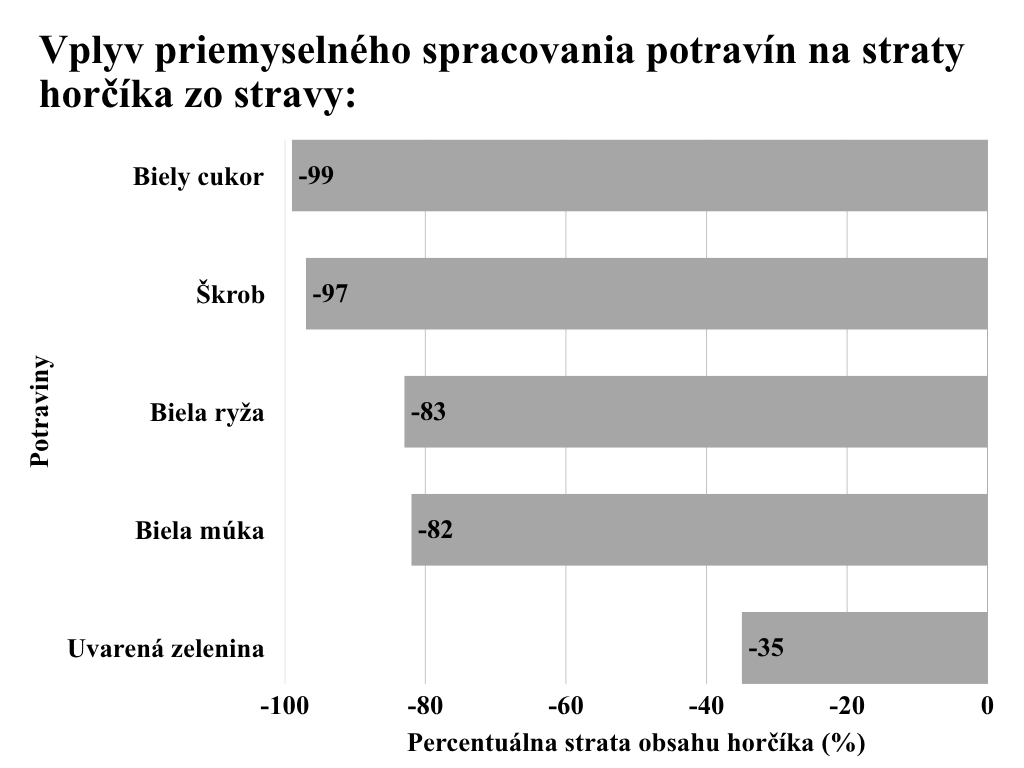
Cazzola et al. (2020) uvádzajú merateľný pokles obsahu horčíka v ovocí a zelenine za posledných 50 rokov, pričom priemyselné spracovanie surovín odstraňuje až 80 % pôvodného množstva tohto minerálu v strave [11]. Niektoré procesy spracovania potravín (varenie, rafinácia a pod.) sú obzvlášť devastačné: biela múka stráca 82 % horčíka, biela ryža 83 %, škrob až 97 % a biely cukor až 99 % [2]. Pokles horčíka v pšenici o 20 % od roku 1968 je pripisovaný kyslej pôde, zriedeniu úrody a nerovnováhe hnojenia (nadmerné použitie dusíka a fosforu, ktoré obmedzujú vstrebanie horčíka) [2]. Tento kumulatívny pokles vyúsťuje do globálnej nutričnej krízy, kde podľa najnovších prieskumov z roku 2025 viac ako 2,4 miliardy ľudí neprijíma horčík v odporúčanom množstve stanoveným na 420 mg/deň pre mužov a 320 mg/deň pre ženy [12].
4.2 Chronický stres ako príčina zníženia hladiny horčíka
Chronická psychická záťaž výrazne ovplyvňuje zásoby horčíka prostredníctvom patofyziologického cyklu vzájomného zosilňovania. Keď je organizmus dlhodobo vystavený tlaku, dôjde k aktivácii stresovej osi HPA (hypotalamus, riadiace centrum autonómneho nervového systému; hypofýza, žľaza regulujúca hormóny; nadobličky, ktoré produkujú hlavný stresový hormón – kortizol), kedy je Mg²⁺ zvýšene vylučovaný močom. Následný pokles sérovej hladiny Mg²⁺ zvyšuje citlivosť stresovej HPA osi, čo má za následok vyššie uvoľňovanie kortizolu a takto sa progresívne prehlbuje deficit minerálu [13].
Súvislosť medzi stresom a poklesom hladiny horčíka potvrdzujú pozorovacie štúdie u vysokoškolských študentov počas skúškového obdobia, kedy priamo súvisel nárast subjektívnej úzkosti so zvýšeným vylučovaním horčíka v moči, pričom po záverečnom skúškovom období bol zaznamenaný pokles jeho zásob v červených krvinkách (erytrocytoch) [13].
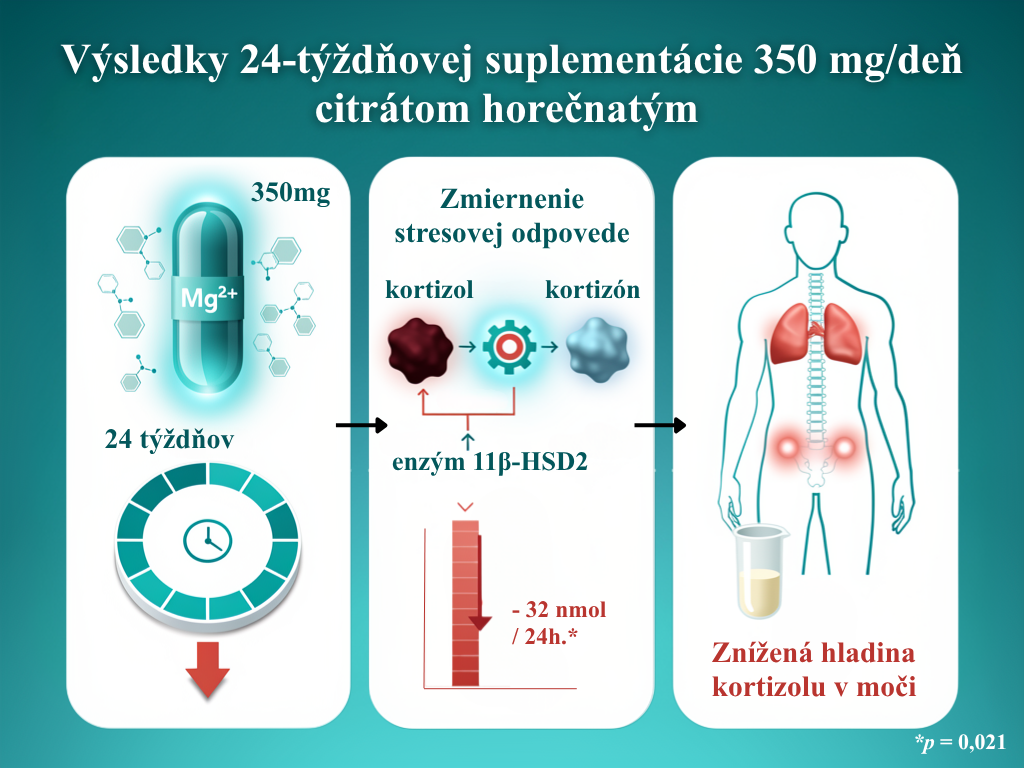
Významný dôkaz o tom, že opačný smer tiež platí, priniesla štúdia od Schutten et al. (2021), ktorá bola realizovaná na 49 ľuďoch s nadváhou alebo miernou obezitou (muži a postmenopauzálne ženy vo veku 45–70 rokov) [14]. Štúdia odhalila, že 24-týždňová suplementácia citrátom horečnatým v dávke 350 mg/deň viedla k štatisticky významnému zníženiu hladiny kortizolu v moči o 32 nmol/24 h oproti placebu (95% CI: −59 až −5 nmol/24 h; p = 0,021). Je to zrejme spôsobené zvýšenou aktivitou enzýmu 11β-HSD2, ktorý zabezpečuje premenu kortizolu na menej aktívny kortizón, čím horčík dokáže prispieť k zmierneniu stresovej odpovede [14].
4.3 Priemyselne spracované potraviny a nerovnováha sodíka voči draslíku
Priemyselne spracované potraviny sa vyznačujú nadbytkom sodíka (Na⁺) a sú chudobné na draslík, čo vedie k aktívnemu narúšaniu bunkovej rovnováhy elektrolytov. Deficit draslíka v strave spúšťa intracelulárnu WNK kinázu (with-no-lysine kináza – regulačný enzým absentujúci lyzínu v aktívnom mieste), ktorá stimuluje transportér NCC (sodíko-chloridový kotransportér) v distálnom nefróne obličky. Vyššia aktivita NCC vedie k zadržiavaniu Na⁺, čo je kľúčovým faktorom vzniku alebo zhoršenia arteriálnej hypertenzie [5]. Štúdia u starších osôb nad 65 rokov zistila, že úprava pomeru Na/K v strave prostredníctvom vyššieho príjmu draslíka sa prejavilo nižším rizikom hypertenzie a kardiovaskulárnych príhod, najmä cievnej mozgovej príhody [15].
4.4 Farmakoterapia ako iatrogénna príčina nedostatku živín
Okrem nutričných a environmentálnych faktorov predstavuje dlhodobé užívanie liekov významné vyčerpávanie množstva horčíka, draslíka a CoQ10 z organizmu.
Kľúčovú úlohu zohrávajú diuretiká (predovšetkým tiazidové a slučkové, napr. furosemid, hydrochlorotiazidum), ktoré zintenzívňujú renálne straty K⁺ a Mg²⁺. Na 25 pacientoch užívajúcich diuretiká po dobu 2–14 rokov bolo v klinickej štúdií preukázané, že hladiny draslíka, horčíka a Na⁺/K⁺-ATPázy v biopsiách kostrového svalu boli výrazne nižšie ako u kontrolnej skupiny aj napriek tomu, že väčšina pacientov užívala samotný draslík. Tento fakt potvrdil, že suplementácia samotným draslíkom bez úpravy deficitu horčíka nepostačuje na obnovu vnútrobunkovej elektrolytovej rovnováhy [16].
Statíny (inhibítory HMG-CoA reduktázy, napr. atorvastatín, rosuvastatín) priamo v pečeňových bunkách blokujú mevalonátovú dráhu, ktorá je potrebná nielen na tvorbu cholesterolu, ale práve aj na produkciu CoQ10, čo sa u predisponovaných jedincov dokáže prejaviť svalovou slabosťou (statínová myopatia) [6]. Podobne pôsobia aj beta-blokátory (napr. metoprolol, bisoprolol, karvedilol) a metformín (najčastejšie predpisované antidiabetikum), ktoré rôznymi biochemickými cestami znižujú dostupnosť CoQ10 v tkanivách [17].
Inhibítory protónovej pumpy (IPP, napr. omeprazol, pantoprazol), ktoré sa užívajú pri ochoreniach hornej časti gastrointestinálneho traktu, znižujú vstrebateľnosť horčíka v tenkom čreve inhibíciou transportérov TRPM6/7, ktoré sú zodpovedné za aktívny transport horčíka do krvi, čo môže vyústiť k závažnej hypomagneziémii [18].
5. Rizikové skupiny
Analýza príčin deficitu priamo vedie k definovaniu rizikových skupín, u ktorých je pravdepodobnosť tohto nedostatku zvýšená a u ktorých je preventívna alebo terapeutická suplementácia nevyhnutným krokom.
1. Pacienti s arteriálnou hypertenziou (vysoký krvný tlak) čelia nasledovným hrozbám:
- spracovaná strava s vysokým obsahom Na⁺ a nízkym obsahom K⁺, ktorá vedie k vysokému nepomeru elektrolytov,
- diuretická liečba vo veľkom prispieva k stratám draslíka a horčíka a kvôli beta-blokátorom je obmedzená produkcia koenzýmu Q10. Preto sú títo pacienti jednou z najrizikovejších skupín z hľadiska deficitu celej trojice spomínaných kľúčových zložiek.
2. Pacienti so srdcovým zlyhávaním a statínovou liečbou - srdcové zlyhávanie je charakterizované dysfunkciou mitochondrií a poškodením tkanív oxidačným stresom. Deficit koenzýmu Q10 je u týchto pacientov aj klinicky skúmaný. Štúdia vykonaná na 120 pacientoch so srdcovým zlyhávaním (Bodea et al., 2025) potvrdila efektivitu užívania CoQ10 v dennej dávke 2 × 60 mg počas 6 mesiacov [6]. Po spomínanej dobe sa touto suplementáciou významne zlepšila ejekčná frakcia ľavej komory (LVEF – percentuálny podiel krvi vytlačenej z ľavej komory pri každom srdcovom sťahu; normálna hodnota ≥ 55 %) a miera deformácie svalu (GLS – miera deformácie srdcového svalu počas systoly; čím je hodnota vyššia v absolútnej hodnote, tým lepšia kontrakcia), čo v praxi znamená silnejšiu a efektívnejšiu funkciu srdca.
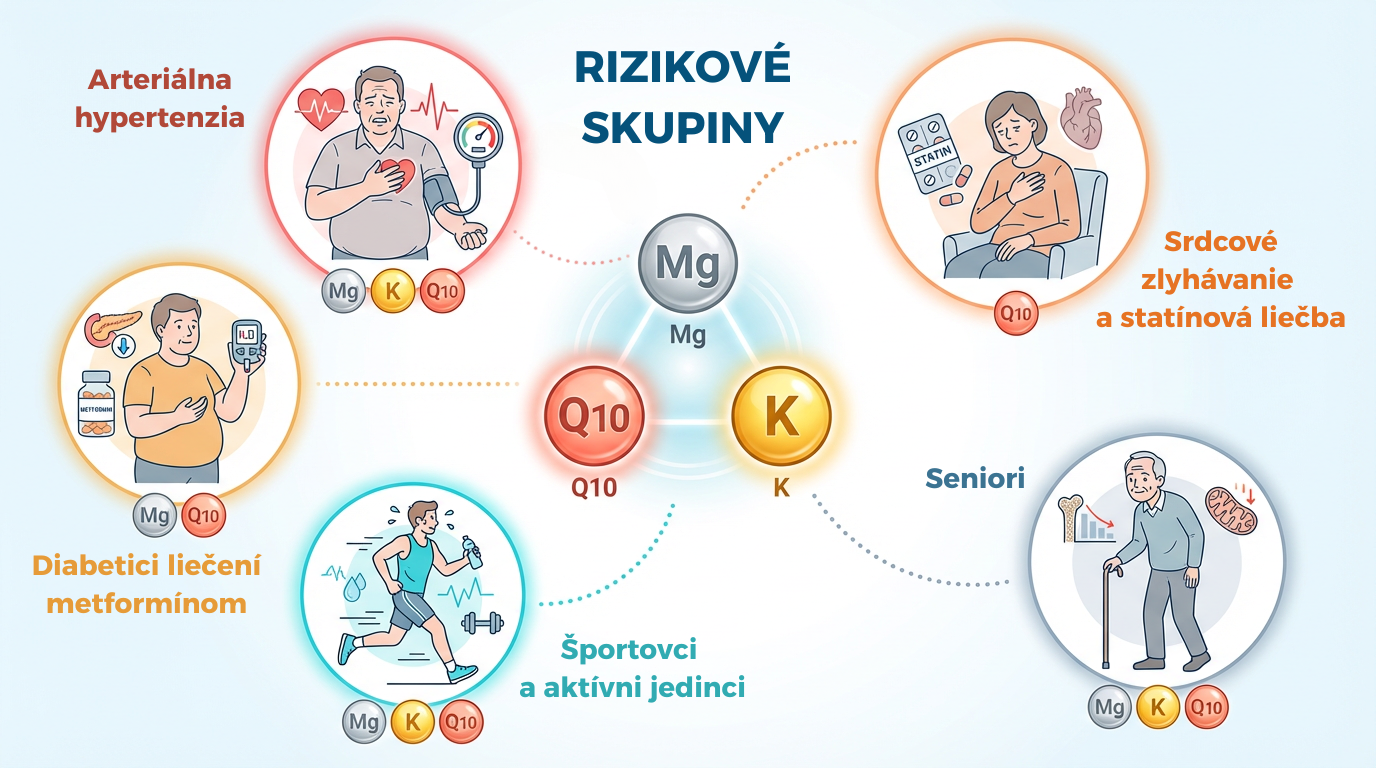
3. Diabetici liečení metformínom - dlhodobé užívanie metformínu je spojené so znížením tvorby koenzýmu Q10 [17]. Navyše, v dôsledku osmotickej diurézy, ktorá je spôsobená vysokou hladinou cukru v krvi, sa zvyšujú renálne straty horčíka.
4. Športovci a fyzicky aktívni jedinci- intenzívna fyzická záťaž zvyšuje nárok na draslík a horčíkz viacerých dôvodov:
- Odporúčaná denná dávka (RVH) horčíka je pre dospelých mužov 350 mg a u dospelých žien to je 300 mg. V štúdií z roku 2025 bolo skúmané, ako namáhavé cvičenie môže o to viac zvýšiť potrebu horčíka u mnohých vrcholových športovcov (vrátane bežcov, basketbalistov, rugby hráčov či gymnastiek) aj o 10-20% ako je RVH kvôli zvýšeným stratám potom a močom [19].
- Metaanalýza 17 randomizovaných kontrolovaných štúdií zahŕňajúca 440 účastníkov preukázala, že suplementácia CoQ10 u športovcov podstatne dokázala znížiť plazmatické hladiny malondialdehyd (MDA, marker oxidačného stresu) o 0,61 μmol/l (95% CI: 1,18 až −0,03; p = 0,04), kreatínkinázy (CK, marker svalového poškodenia) o 71,81 IU/l (95% CI: 124,33 až −19,3; p = 0,012) a laktátdehydrogenázy (LDH, biomarker poškodenia svalov) o 69,99 IU/l (95% CI: 131,93 až −8,05; p = 0,033) [20].
5. Seniori - vekom dochádza k poklesu produkcie koenzýmu Q10, znížuje sa schopnosť vstrebateľnosti horčíka pri achlorhydrii (oslabenej produkcii žalúdočnej kyseliny) a časté užívanie množstva liekov súčasne kumulatívne zvyšujú riziko deficitu celej trojice. Štúdia uskutočnená na 71 osobách nad 65 rokov zistila, že vyššie plazmatické hladiny CoQ10 boli spojené s nižším kardiovaskulárnym rizikom a vyššou pohybovou aktivitou spôsobenou silnejšou svalovou kapacitou [21].
6. Prečo je suplementácia v súčasnosti dôležitá
Po objasnení príčin nedostatku spomínaných kľúčových zložiek a rizikových skupín vyvstáva otázka, do akej miery je možné pokryť potreby týchto látok bežnou stravou a kedy je nutné zvážiť suplementáciu.
6.1 Nedostatočnosť živín z potravinových zdrojov
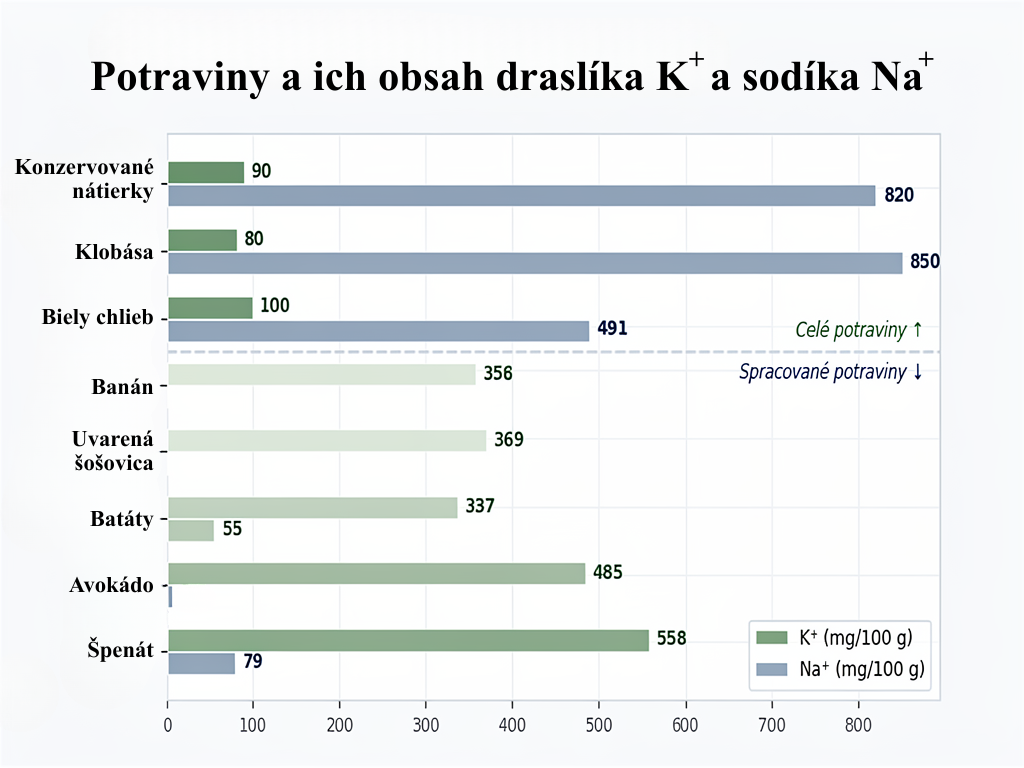
Dosiahnutie odporúčaného denného príjmu draslíka (3 500–4 700 mg/deň) stravou je v súčasnosti problematické. Pokrytie takejto dávky pomocou potravín bohatých na draslík, ako je napríklad banán (obsahuje približne 360–400 mg draslíka), by si vyžadovalo konzumáciu 9 až 12 kusov denne, čo je dlhodobo neudržateľné z hľadiska obsahu jednoduchých cukrov a kalorického príjmu. Navyše, ďalšie potravinové zdroje bohaté na K⁺ ako batáty, strukoviny, avokádo, tmavá listová zelenina sú síce dostupné, ale v modernej strave sú často vytláčané priemyselne upravenými potravinami s vysokým podielom sodíka.
Podobná situácia nastáva pri horčíku, kde merateľný pokles jeho koncentrácie v obilninách a zelenine spôsobuje, že ani vyvážená konzumácia potravín považovaných za bohaté zdroje horčíka nemusí pokryť jeho odporúčaný denný príjem [2, 9].
Pri koenzýme Q10 je situácia špecifická tým, že jeho množstvá prijímané potravou – predovšetkým prostredníctvom orgánového mäsa, mastných rýb a orechov – sú výrazne nižšie ako množstvá používané v klinických štúdiách, a vlastná biosyntéza s vekom nezvratne slabne. Výskum zameraný na tkanivové biopsy kože od 23 darcov rôzneho veku preukázal, že mitochondriálna respirácia a syntéza ATP v súvislosti s vekom významne klesali. Avšak experimentálne podanie ubichinolu tieto parametre zlepšilo, čím sa potvrdilo, že vekom podmienená mitochondriálna dysfunkcia súvisí s poklesom CoQ10 a tento proces je možné prostredníctvom cielenej suplementácie sčasti zvrátiť [18].
6.2 Biologická dostupnosť ako kľúč efektivity suplementácie
Dávka zložky, ktorá je uvedená na obale výživového doplnku, nezodpovedá skutočnému množstvu, ktoré sa dokáže bez problémov vstrebať do krvného obehu a buniek. Biologická dostupnosť a vstrebateľnosť zložky sú kriticky závislé od ich chemickej formy.
Formy horčíka:
Anorganické formy (napr. oxid horečnatý; síran horečnatý) obsahujú vysoké percento elementárneho horčíka, avšak ich slabá rozpustnosť vo vode a závislosť od pH žalúdočnej kyseliny význačne limitujú ich absorpciu.
Organické formy (napr. citrát horečnatý; diglycinát horečnatý; malát horečnatý) sú chelátové zlúčeniny, v ktorých sa horčík viaže na organickú kyselinu alebo aminokyselinu, čím sa zvyšuje ich rozpustnosť a znižuje závislosť absorpcie od pH žalúdočnej kyseliny.
- Diglycinát horečnatý (bisglycinát) - mnohé klinické výskumy konštatujú, že táto forma má najvyššiu biologickú dostupnosť a najnižší výskyt gastrointestinálnych nežiaducich vplyvov. Vstrebáva sa čiastočne aj cez dipeptidový transportér PEPT1 nezávislý od hladiny horčíka v sére, čo ho predurčuje pre osoby s narušenou absorpciou alebo zníženou produkciou žalúdočnej kyseliny [7]. Viac sa o tejto forme horčíka môžete dočítať v našom blogovom článku: “Sú "najlepšie magnéziá" skutočne najlepšie? - Vysvetlenie mýtu, ktorý zaplavil trh”.
- Malát horečnatý (jablčnan horečnatý) je preferovaný pri stavoch chronickej energetickej deficiencie, keďže malátová časť molekuly dokáže vstúpiť priamo do Krebsovho cyklu.
- Taurát horečnatý je kombináciou atómu horčíka s aminokyselinou taurín. Spája sa predovšetkým s priaznivým kardiovaskulárnym pôsobením a preto je diskutovaný najmä v kardiologickom kontexte [7].
Formy draslíka:
Pri bežnej suplementácií draslíkom je vhodné zvoliť organické formy s dobrou biologickou dostupnosťou a priaznivým gastrointestinálnym profilom.
- Glukonát draselný vykazuje približne až 94 % vstrebateľnosť, ktorá sa dá dobre porovnať s potravinovými zdrojmi K⁺ a má dobrú znášanlivosť organizmom [23].
- Citrát draselný je rovnako vysoko vstrebateľnou formou a má navyše alkalinizačný účinok na moč, čo je výhodné u pacientov s urolitiázou (obličkovými kameňmi) [24].
- Uhličitan a bikarbonát draselný sú skúmané v kontexte ochranykostnej minerálnej hustoty [24].
Hoci je deficit draslíka bežný, k jeho dopĺňaniu prostredníctvom ýživových doplnkov sa pristupuje opatrne. Voľnopredajné doplnky s K⁺ sú v mnohých krajinách EÚ limitované na 99 mg elementárneho draslíka na dávku. Dôvodom je riziko hyperkaliémie (nadmerne zvýšenej hladiny draslíka v krvi) u rizikových pacientov [24].
Formy CoQ10:
Z hľadiska suplementácie predstavuje ubichinolefektívnejšiu alternatívu k ubichinónu, keďže vstupuje priamo do dýchacieho reťazca bez nutnosti predchádzajúcej enzymatickej redukcie. Táto vlastnosť je kľúčová najmä u seniorov a pacientov so závažnou mitochondriálnou dysfunkciou (napr. Pacienti so srdcovým zlyhávaním či liečbou statínmi), u ktorých je schopnosť endogénnej premeny foriem koenzýmu z ubichinónu na ubichinol obmedzená a preto je pre tieto skupiny suplementácia ubichinolom fyziologicky opodstatnenejšia. Keďže ide o lipofilnú (v tukoch rozpustnú) molekulu, absorpcia koenzýmu Q10 je podmienená prítomnosťou tukov v potrave, respektíve suplementáciou koenzýmu Q10 v olejových kapsuliach, známych ako softgél.
7. Klinické odporúčania a bezpečnosť suplementácie
Suplementáciu kombináciou Mg–K–CoQ10 je nutné prispôsobiť individuálnemu profilu osoby, pri zohľadnení komorbidít, farmakoterapie a celkového nutričného stavu. Nasledujúce vymenované dávky vychádzajú z parametrov použitých v citovaných klinických štúdiách a z odporúčaní odborníkov:
- Horčík: 300 mg elementárneho Mg²⁺/deň v organickej forme, prednostne diglycinát horečnatý. Vzhľadom na relaxačné pôsobenie na svalstvo a pozitívny efekt na kvalitu spánku sa táto forma odporúča užívať vo večerných hodinách. U pacientov so zníženou funkciou obličiek je užívanie kontraindikované bez lekárskeho dohľadu pre riziko akumulácie horčíka a vzniku hypermagneziémie.
- Draslík: U väčšiny zdravých jedincov predstavuje primárny prístup zvýšenie príjmu K⁺ prostredníctvom nutrične bohatých potravín na tento minerál (strukoviny, listová zelenina, avokádo, sladké zemiaky) v kombinácii s odporúčanými dávkami organických solí, ako sú citrát alebo glukonát draselný, ktoré sú dobre tolerované a biologicky dostupné. Naopak vyššie dávky vo forme farmaceutických preparátov by mali byť vedené lekárom, keďže hyperkaliémia je potenciálne život ohrozujúca (najmä u pacientov s renálnou insuficienciou, diabetes mellitus alebo u osôb užívajúcich inhibítory RAAS (renín-angiotenzín-aldosterónového systému – hormónového systému regulujúceho krvný tlak a elektrolytovú rovnováhu).
- Koenzým Q10 (ubichinol): Pre zdravých dospelých jedincov je vhodné množstvo 50 mg/deň; vyššie dávky 200–600 mg/deň je nutné konzultovať s lekárom. Aplikácia s jedlom obsahujúcim tuky je nevyhnutná na adekvátne vstrebanie.
Horčík, draslík a koenzým Q10 tvoria biochemicky prepojenú jednotku, ktorej primárnou funkciou je riadenie bunkovej energetiky, mitochondriálnej rovnováhy a elektrolytovej stability. Deficit horčíka narúša biologickú aktivitu ATP a spôsobuje sekundárne straty draslíka. Nedostatok koenzýmu Q10 priamo blokuje prenos elektrónov v dýchacom reťazci, čím drasticky znižuje produkciu ATP. Nízka hladina draslíka následne destabilizuje membránový potenciál srdca, svalov a nervov. Tieto mechanizmy sa v patologickom procese vzájomne posilňujú.
Plošný výskyt deficitu v dnešnej dobe je výsledkom chronického stresu, starnutia organizmu, vyčerpania kľúčových látok z pôdy a ultra-spracovanými potravinami. Pre korigovanie tohto deficitu je nevyhnutná cielená a súbežná suplementácia všetkých troch zložiek, nakoľko ich funkčná previazanosť neumožňuje izolovanú nápravu hladiny jednej z nich bez prítomnosti ostatných.
Bibliografické údaje
[1] Kröse, J. L., & de Baaij, J. H. F. (2024). Magnesium biology. Nephrology, dialysis, transplantation : official publication of the European Dialysis and Transplant Association - European Renal Association, 39(12), 1965–1975. DOI: 10.1093/ndt/gfae134.
[2] Fiorentini, D., Cappadone, C., Farruggia, G., & Prata, C. (2021). Magnesium: Biochemistry, Nutrition, Detection, and Social Impact of Diseases Linked to Its Deficiency. Nutrients, 13(4), 1136. DOI: 10.3390/nu13041136.
[3] Romani A. M. (2011). Cellular magnesium homeostasis. Archives of biochemistry and biophysics, 512(1), 1–23. DOI: 10.1016/j.abb.2011.05.010.
[4] Alosaimi M. M, Monther N. A, Abdulmajeed A, Mutlaq A. (2025). Hypokalemia: Pathophysiology, Diagnosis, and Management. J Surg. 10:11511. DOI:10.29011/2575-9760.011511.
[5] Chan, R. J., Parikh, N., Ahmed, S., Ruzicka, M., & Hiremath, S. (2024). Blood Pressure Control Should Focus on More Potassium: Controversies in Hypertension. Hypertension (Dallas, Tex.: 1979), 81(3), 501–509. DOI: 10.1161/HYPERTENSIONAHA.123.20545.
[6] Bodea, O., Boia, E. R., Craciun, L. M., Valcovici, M. D., Motofelea, A. C., Munteanu, A. M., Streian, C. G., Pop, G. N., & Dragan, S. R. (2025). Effect of Coenzyme Q10 Supplementation on Cardiac Function and Quality of Life in Patients with Heart Failure: A Randomized Controlled Trial. Journal of Clinical Medicine, 14(11), 3675. DOI: 10.3390/jcm14113675.
[7] Cepeda, V., Ródenas-Munar, M., García, S., Bouzas, C., & Tur, J. A. (2025). Unlocking the Power of Magnesium: A Systematic Review and Meta-Analysis Regarding Its Role in Oxidative Stress and Inflammation. Antioxidants (Basel, Switzerland), 14(6), 740. DOI:10.3390/antiox14060740.
[8] Nankivell, M. C., Rosenfeldt, F., Pipingas, A., Pase, M. P., Reddan, J. M., & Stough, C. (2025). Coenzyme Q10 and Cognition: A Review. Nutrients, 17(17), 2896. DOI: 10.3390/nu17172896.
[9] Tarleton, E. K., Littenberg, B., MacLean, C. D., Kennedy, A. G., & Daley, C. (2017). Role of magnesium supplementation in the treatment of depression: A randomized clinical trial. PloS one, 12(6), e0180067. DOI: 10.1371/journal.pone.0180067.
[10] Moabedi, M., Aliakbari, M., Erfanian, S., & Milajerdi, A. (2023). Magnesium supplementation beneficially affects depression in adults with depressive disorder: a systematic review and meta-analysis of randomized clinical trials. Frontiers in psychiatry, 14, 1333261. DOI: 10.3389/fpsyt.2023.1333261.
[11] Cazzola, R., Della Porta, M., Manoni, M., Iotti, S., Pinotti, L., & Maier, J. A. (2020). Going to the roots of reduced magnesium dietary intake: A tradeoff between climate changes and sources. Heliyon, 6(11), e05390. DOI: 10.1016/j.heliyon.2020.e05390.
[12] Zhang, W., & Zhao, Y. (2025). Global Dietary Magnesium Deficiency: Prevalence, Underlying Causes, Health Consequences, and Strategic Solutions. International journal for vitamin and nutrition research. 95(6), 46828. DOI: 10.31083/IJVNR46828.
[13] Pickering, G., Mazur, A., Trousselard, M., Bienkowski, P., Yaltsewa, N., Amessou, M., Noah, L., & Pouteau, E. (2020). Magnesium Status and Stress: The Vicious Circle Concept Revisited. Nutrients, 12(12), 3672. DOI: 10.3390/nu12123672.
[14] Schutten JC, Joris PJ, Minović I, et al. Long-term magnesium supplementation improves glucocorticoid metabolism: A post-hoc analysis of an intervention trial. Clin Endocrinol (Oxf).2021;94:150–157. DOI: 10.1111/cen.14350.
[15] Gonçalves, C., & Abreu, S. (2020). Sodium and Potassium Intake and Cardiovascular Disease in Older People: A Systematic Review. Nutrients, 12(11), 3447. DOI: 10.3390/nu12113447.
[16] Dorup I, et al. Reduced concentrations of potassium, magnesium, and sodium-potassium pumps in human skeletal muscle during treatment with diuretics. BMJ. 1988;296(6620):455–458. DOI: 10.1136/bmj.296.6620.455.
[17] Raizner, A. E., & Quiñones, M. A. (2021). Coenzyme Q10 for Patients With Cardiovascular Disease: JACC Focus Seminar. Journal of the American College of Cardiology, 77(5), 609–619. DOI: 10.1016/j.jacc.2020.12.009.
[18] Schniertshauer, D., Gebhard, D., & Bergemann, J. (2018). Age-Dependent Loss of Mitochondrial Function in Epithelial Tissue Can Be Reversed by Coenzyme Q10. Journal of aging research, 2018, 6354680. DOI: 10.1155/2018/6354680.
[19] Dominguez, L. J., Veronese, N., Ragusa, F. S., Baio, S. M., Sgrò, F., Russo, A., Battaglia, G., Bianco, A., & Barbagallo, M. (2025). The Importance of Vitamin D and Magnesium in Athletes. Nutrients, 17(10), 1655. DOI: 10.3390/nu17101655.
[20] Qu, H., & Qu, Y. (2025). Can coenzyme Q10 supplementation reduce exercise-induced muscle damage and oxidative stress in athletes? A systematic review and meta-analysis. Complementary therapies in clinical practice, 60, 102001. DOI: 10.1016/j.ctcp.2025.102001.
[21] Barea-Rodriguez EJ, et al. Levels of Plasma Coenzyme Q10 Are Associated with Physical Capacity and Cardiovascular Risk in the Elderly. Antioxidants. 2022;11(3):490. DOI: 10.3390/antiox11020279
[23] Macdonald-Clarke CJ, Martin BR, McCabe LD, et al. Bioavailability of potassium from potatoes and potassium gluconate: a randomized dose response trial. The American Journal of Clinical Nutrition. 2016 Aug;104(2):346-353. DOI: 10.3945/ajcn.115.127225.
[24] NIH Office of Dietary Supplements. Potassium — Health Professional Fact Sheet. Bethesda: National Institutes of Health; 2024. Dostupné na: https://ods.od.nih.gov/factsheets/Potassium-HealthProfessional/.ň
Zdroje obrázkov: kombinácia ilustrácií generovaných umelou inteligenciou (AI) a originálnej autorskej tvorby.
